Você já parou para pensar por que o café quente esfria, ou como um motor consegue mover um carro? A resposta para essas e muitas outras perguntas está na termodinâmica. Esta fascinante área da física estuda o calor e sua relação com outras formas de energia e trabalho. Longe de ser um conceito abstrato restrito a cientistas, a termodinâmica permeia nossa existência, desde o funcionamento do seu corpo até a geração de energia em larga escala. Entender suas leis fundamentais não é apenas uma curiosidade acadêmica; é uma forma de desvendar os princípios que governam o universo ao nosso redor. Prepare-se para uma jornada descomplicada pelas quatro leis essenciais que explicam como a energia se comporta e transforma.
O Que É Termodinâmica e Por Que Ela Importa?
A termodinâmica é, em sua essência, a ciência das transformações de energia. Ela nos ajuda a compreender como a energia se move e se altera entre diferentes estados e sistemas. Sem ela, não teríamos refrigeradores, motores a combustão, usinas de energia, nem mesmo a complexidade da vida biológica. Imagine um mundo onde o calor não se movesse, ou onde a energia pudesse simplesmente surgir do nada ou desaparecer. Seria um universo caótico e imprevisível. As leis da termodinâmica, no entanto, fornecem a estrutura para entender essa orquestra de energia, permitindo-nos prever o comportamento de sistemas e desenvolver tecnologias inovadoras. Elas são a base para a engenharia, a química, a biologia e até mesmo a cosmologia, demonstrando sua relevância universal.
A Lei Zero da Termodinâmica: O Princípio do Equilíbrio Térmico
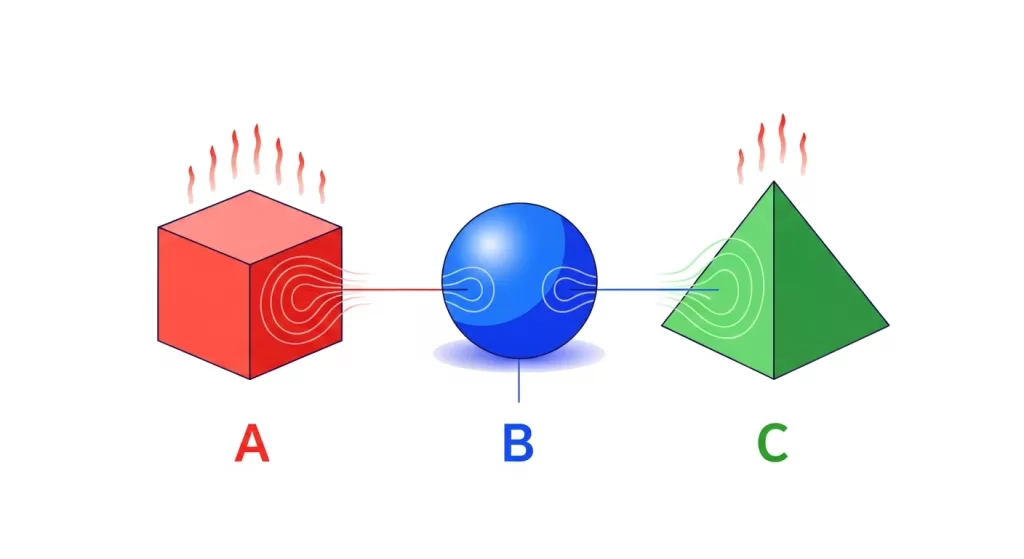
Pode parecer estranho que a primeira lei que estudamos seja a ‘Lei Zero’, mas sua importância fundamental para a definição de temperatura a posicionou antes das outras. A Lei Zero da Termodinâmica estabelece que, se dois sistemas estão em equilíbrio térmico com um terceiro sistema, então eles também estão em equilíbrio térmico entre si. Em termos mais simples, se o corpo A tem a mesma temperatura que o corpo B, e o corpo B tem a mesma temperatura que o corpo C, então o corpo A necessariamente tem a mesma temperatura que o corpo C. Este princípio é o que permite a existência de termômetros! Quando você mede sua febre, o termômetro (sistema B) entra em equilíbrio térmico com seu corpo (sistema A). Se o termômetro já foi calibrado com um padrão (sistema C), ele pode indicar sua temperatura com precisão. É uma base intuitiva, mas crucial, para todas as medições térmicas e para a compreensão de como o calor se distribui até que não haja mais fluxos espontâneos de energia.
A Primeira Lei da Termodinâmica: A Conservação da Energia
A Primeira Lei da Termodinâmica é, sem dúvida, uma das leis mais fundamentais da física: a conservação da energia. Ela afirma que a energia não pode ser criada nem destruída, apenas transformada de uma forma para outra. No contexto de um sistema termodinâmico, isso significa que a variação na energia interna de um sistema (ΔU) é igual ao calor adicionado ao sistema (Q) menos o trabalho realizado pelo sistema (W): ΔU = Q – W. Ou seja, se você adiciona calor a um sistema, essa energia pode aumentar sua energia interna (tornando-o mais quente), ou pode ser usada para realizar trabalho. Por exemplo, em uma máquina a vapor, o calor da combustão da lenha ou do carvão é usado para aquecer a água e gerar vapor, que por sua vez empurra um pistão (realizando trabalho). A energia total antes e depois do processo permanece constante, apenas muda de forma, como de energia química para térmica e depois mecânica. Essa lei desmascara a ideia de máquinas de movimento perpétuo de primeira espécie, que prometem gerar energia do nada, algo impossível de acordo com este princípio inviolável.
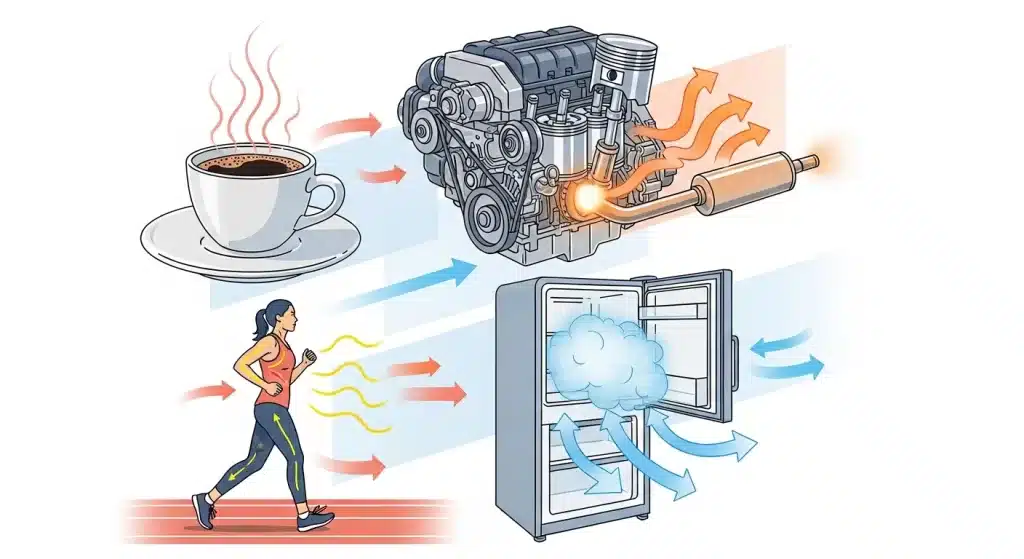
Para ilustrar melhor, pense em uma lâmpada. Ela não cria energia, mas converte energia elétrica em luz e calor. Um atleta consome alimentos (energia química) e os transforma em energia mecânica para correr e calor para manter sua temperatura corporal. Cada processo energético que observamos no universo segue essa regra rigorosa. A compreensão da conservação da energia é vital para a engenharia de sistemas eficientes, desde motores de automóveis até geradores elétricos, garantindo que minimizemos o desperdício e otimizemos o uso dos recursos energéticos disponíveis. É a base para a contabilidade energética de qualquer processo físico ou químico.
A Segunda Lei da Termodinâmica: A Entropia e a Direção dos Processos
A Segunda Lei da Termodinâmica é talvez a mais profunda e, para muitos, a mais desafiadora de se compreender plenamente, mas é também a que explica a ‘direção’ dos eventos no universo. Ela introduz o conceito de entropia, que pode ser entendida como uma medida do nível de desordem ou aleatoriedade em um sistema. A lei afirma que a entropia total de um sistema isolado nunca diminui com o tempo; ela sempre aumenta para processos espontâneos e permanece constante para processos reversíveis. Em termos práticos, o universo, como um todo, tende a um estado de maior desordem. Pense em um copo que cai e se quebra: a quebra aumenta a desordem (entropia), e nunca vemos os pedaços se juntarem espontaneamente para formar o copo novamente. O calor sempre flui de um corpo mais quente para um corpo mais frio, nunca o contrário, a menos que trabalho seja realizado sobre o sistema (como em um refrigerador). Essa lei é a ‘flecha do tempo’, indicando que os processos no universo têm uma direção preferencial. Ela também impõe um limite fundamental à eficiência de qualquer máquina térmica, afirmando que é impossível converter 100% do calor em trabalho útil, pois sempre haverá alguma perda de energia na forma de calor não utilizável, aumentando a entropia do ambiente.
A irreversibilidade é a marca registrada da Segunda Lei. Misturar café com leite aumenta a entropia; desmisturar é praticamente impossível sem um gasto considerável de energia. Da mesma forma, nosso próprio corpo e todos os sistemas biológicos lutam constantemente contra o aumento da entropia, exigindo um suprimento contínuo de energia para manter sua estrutura e função ordenadas. Em uma escala cósmica, essa lei prevê o eventual ‘frio’ do universo, onde todas as diferenças de temperatura serão erradicadas e a energia estará tão dispersa que nenhum trabalho útil poderá ser extraído, um estado conhecido como ‘morte térmica’. É uma lei que nos força a confrontar os limites fundamentais da energia e da organização.
A Terceira Lei da Termodinâmica: O Zero Absoluto e a Impossibilidade
A Terceira Lei da Termodinâmica aborda o comportamento da entropia à medida que a temperatura de um sistema se aproxima do zero absoluto. O zero absoluto, equivalente a 0 Kelvin ou -273.15 °C, é a temperatura teórica na qual todo o movimento atômico e molecular cessa completamente, e um sistema atinge seu estado fundamental de menor energia. A Terceira Lei afirma que a entropia de um cristal perfeito em zero absoluto é zero. Mais importante ainda, ela estabelece que é impossível resfriar um sistema até o zero absoluto em um número finito de passos. Por mais que tentemos remover calor de um sistema, sempre haverá uma pequena quantidade residual de energia, tornando o zero absoluto uma fronteira inatingível. Conforme nos aproximamos do zero absoluto, a energia residual se torna cada vez mais difícil de ser extraída, exigindo esforços cada vez maiores para reduções incrementais de temperatura. Esta lei tem implicações cruciais na criogenia, o estudo e aplicação de temperaturas extremamente baixas. Cientistas utilizam tecnologias avançadas para se aproximar do zero absoluto, explorando fenômenos quânticos como a supercondutividade e a superfluidez, que ocorrem nessas condições extremas. Embora nunca possamos alcançar o zero absoluto, a busca por temperaturas ultra-baixas continua a desvendar novas e fascinantes propriedades da matéria, impulsionando avanços tecnológicos e científicos.
Termodinâmica no Dia a Dia: Exemplos Práticos
As leis da Termodinâmica não são apenas equações de livros; elas estão em ação constante ao nosso redor. O seu refrigerador, por exemplo, funciona contra a tendência natural do calor (Segunda Lei), usando trabalho (energia elétrica) para mover o calor de dentro para fora, mantendo seus alimentos frescos. Um aquecedor de água elétrico segue a Primeira Lei, convertendo energia elétrica em calor para aquecer a água, sem que a energia se perca. Quando você cozinha, a transferência de calor do fogão para a panela e para o alimento é um processo termodinâmico contínuo. Mesmo o nosso corpo é uma máquina termodinâmica complexa, convertendo a energia química dos alimentos em calor para manter a temperatura corporal e em trabalho mecânico para o movimento e outras funções vitais, sempre produzindo entropia ao longo do caminho. Os motores de carros, as turbinas de aviões e as usinas de energia são todas maravilhas da engenharia termodinâmica, projetadas para otimizar a conversão de calor em trabalho útil, dentro dos limites impostos pela Segunda Lei. A termodinâmica também é essencial para entender fenômenos naturais como o clima, a formação de estrelas e a evolução de ecossistemas. Em cada canto do nosso mundo, do microscópico ao macroscópico, as leis da Termodinâmica orquestram o fluxo de energia, definindo o que é possível e o que não é.
Dominando o Fluxo de Energia
As leis da Termodinâmica, embora possam parecer complexas à primeira vista, são pilares fundamentais para a nossa compreensão do universo. Desde a Lei Zero, que estabelece a base para a temperatura, passando pela Primeira Lei, que garante a conservação da energia, até a Segunda Lei, que define a direção dos processos e o inevitável aumento da desordem, e finalmente a Terceira Lei, que nos fala sobre os limites do resfriamento, todas elas pintam um quadro coeso de como a energia funciona. Elas explicam por que certas coisas acontecem espontaneamente e outras não, e por que a eficiência perfeita é uma miragem. Ao descomplicar a termodinâmica, percebemos que essas leis não são apenas para físicos; elas são uma lente através da qual podemos observar e entender melhor o mundo em que vivemos, desde a mais simples xícara de café até as mais avançadas tecnologias que impulsionam a sociedade moderna. Dominar esses conceitos é dominar a essência do fluxo de energia que sustenta toda a existência.
